Oficina de Ensayos Clínicos (OEC)
En octubre de 2021, la Oficina de Ensayos Clínicos fue creada durante la reestructuración del Vicerrectorado de Investigación, aprobada en Consejo Universitario. Se encuentra bajo la Dirección Universitaria de Asuntos Regulatorios de la Investigación (DUARI).
Nosotros
La Oficina de Ensayos Clínicos (OEC) es responsable de asegurar que la Universidad Peruana Cayetano Heredia cumpla sus funciones como patrocinador o representante legal de un patrocinador extranjero en ensayos clínicos, en cumplimiento con las Buenas Prácticas Clínicas, los principios éticos y la normativa nacional vigente.
Asimismo, la OEC brinda soporte técnico a los centros de investigación bajo la jurisdicción de Cayetano Heredia ante el Instituto Nacional de Salud para la ejecución de ensayos clínicos, conforme a la normativa aplicable.
Regulación
| Los ensayos clínicos en el Perú están regulados por el Reglamento de Ensayos Clínicos, que establece los requisitos éticos y regulatorios para su autorización y ejecución. La OEC de Cayetano Heredia, vela por el cumplimiento de la normativa nacional y de su Política de Responsabilidad en la Gestión y Ejecución de Ensayos Clínicos. |
Regulación Nacional

Reglamento de Ensayos Clínicos
Norma que regula la autorización, ejecución y supervisión de los ensayos clínicos en el Perú, garantizando la protección de los participantes y la calidad científica.
Regulación Institucional

Política Institucional
Lineamientos internos que establecen las responsabilidades de Cayetano en la gestión y ejecución de los ensayos clínicos bajo su patrocinio o representación.
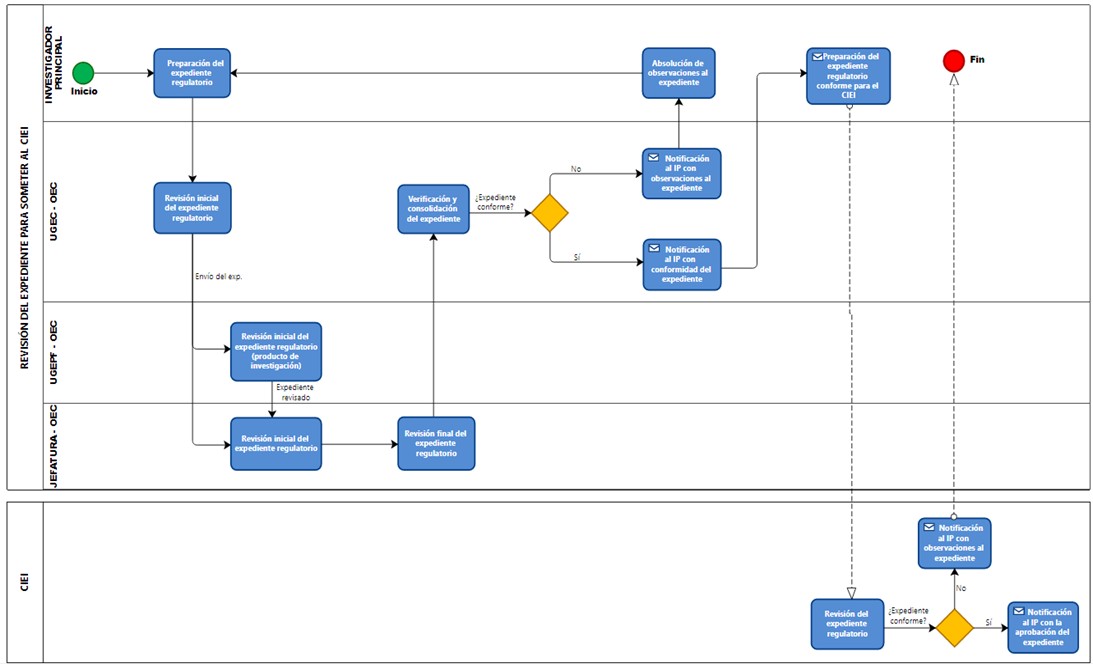
Flujograma
La OEC pone a disposición un flujograma referencial que describe el proceso interno de aprobación del expediente de un ensayo clínico en Cayetano Heredia:
Unidades de la Oficina de Ensayos Clínicos (OEC)
Unidades de la Oficina de Ensayos Clínicos (OEC)
La OEC desarrolla sus funciones a través de las siguientes unidades operativas:
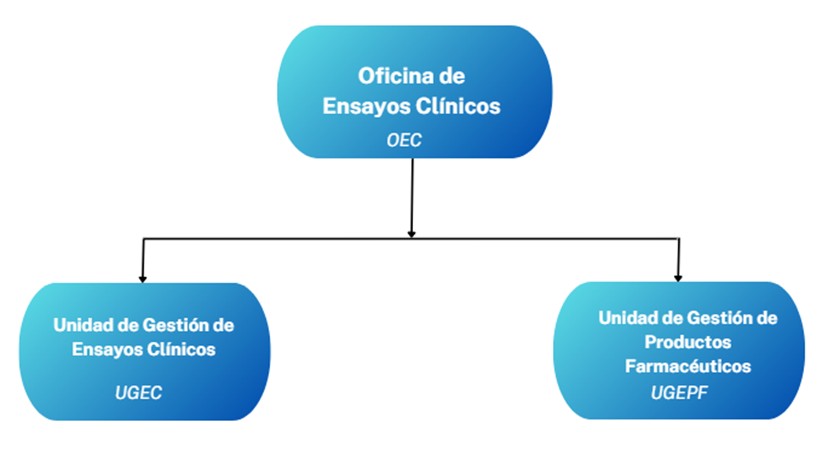
Unidad de Gestión de Productos Farmacéuticos (UGEPF)
Se encarga de la gestión, supervisión y manejo adecuado del producto de investigación en los ensayos clínicos patrocinados por Cayetano, conforme a las Buenas Prácticas Clínicas, Buenas Prácticas de Manufactura, Buenas Prácticas de Almacenamiento y Buenas Prácticas de Distribución y Transporte. Realiza actividades de verificación, control y aseguramiento de calidad de la documentación relacionada al producto de investigación, en concordancia con el protocolo de estudio y la normativa vigente. Asimismo, brinda soporte técnico a los centros e institutos de Cayetano Heredia en temas vinculados al producto de investigación durante la ejecución de los ensayos clínicos.
Unidad de Gestión de Ensayos Clínicos (UGEC)
Es responsable de la gestión administrativa y regulatoria de los ensayos clínicos patrocinados o representados por Cayetano. Brinda soporte a los centros de investigación durante las diferentes etapas del estudio y realiza actividades de verificación y control de calidad de la documentación regulatoria, asegurando el cumplimiento de las Buenas Prácticas Clínicas, los lineamientos éticos y la normativa aplicable.

Formularios del INS
Los procedimientos regulatorios de los ensayos clínicos en el Perú se gestionan mediante formularios oficiales del INS. Desde esta sección se brinda acceso directo a la plataforma del INS, donde se encuentran los formatos y herramientas vigentes.
- Autorización de un ensayo clínico
- Ampliación de centros de investigación
- Ampliación o modificación del listado de suministros a importar
- Cambio de patrocinador u organización de investigación por contrato (OIC)
- Cambio de investigador principal
- Extensión del tiempo de realización del ensayo clínico
- Cierre de centro de investigación
- Suspensión y cancelación del ensayo clínico
- Solicitud de enmiendas
- Gestión de notificaciones de un ensayo clínico
- Desviaciones
- Informe de avances
- Informe final de centro de investigación
- Inicio y término de enrolamiento
- Presentación de informe final nacional e internacional
- Registro de patrocinador extranjero
- Consultas externas
- Soporte en gestión de documentos para un ensayo clínico
- Manejo del producto de investigación
* Los formularios son administrados y actualizados por el INS.
Ensayos clínicos
| AÑO | PATROCINADOR | ROL DE UPCH | FINANCIADOR | TÍTULO DEL ENSAYO CLÍNICO | ESTADO | |
| 2025 | Universidad Peruana Cayetano Heredia | Patrocinador | National Institutes of Health (NIH) | Ensayo clínico controlado, aleatorizado, multicéntrico, de regímenes de dosis única y múltiple de oxfendazol para la neurocisticercosis parenquimal leve (una o dos lesiones). | Aprobado por el INS el 18/03/2025 Vigencia: 5 años | Autorizado, en implementación |
| 2024 | Los Regentes de la Universidad de California | Representante Legal en Perú del Patrocinador extranjero | National Institutes of Health (NIH) | Administración de medicación en masa focal para la eliminación de malaria vivax (FLAME): un estudio pragmático controlado aleatorizado por conglomerados en Perú. | Aprobado por el INS el 21/02/2024 Vigencia: 5 años | Autorizado, en ejecución |
| 2023 | Universidad del Sur de California | Representante Legal en Perú del Patrocinador extranjero | National Institutes of Health (NIH) | Ensayo clínico que compara la eficacia de la cefixima frente a la penicilina G para el tratamiento de la sífilis temprana. | Aprobado por el INS el 25/09/2023 Vigencia: 3 años | Cancelado |
| 2022 | Universidad Peruana Cayetano Heredia | Patrocinador | National Institutes of Health (NIH) | Estudio de no-inferioridad, controlado, aleatorizado, simple ciego, para comparar esquemas de una y dos dosis de oxfendazol versus un esquema de dos dosis de triclabendazol para tratar fascioliasis crónica. | Aprobado por CIEI el 12/02/ 2022 | Autorizado |
Centros de Investigación

“CENTRO DE ESTUDIOS CLÍNICOS – UPCH” (RCI-33)
Centro activo y habilitado para realizar ensayos clínicos en la especialidad médica de:


“CENTRO DE INVESTIGACIÓN PARA ENSAYOS CLÍNICOS UPCH” (RCI-35)
Centro activo y habilitado para realizar ensayos clínicos en las especialidades médicas de:

Recursos
Los siguientes documentos constituyen recursos normativos y técnicos esenciales para la adecuada gestión y ejecución de los ensayos clínicos en Cayetano Heredia:
Entrenamientos
La OEC promueve el fortalecimiento de capacidades en investigación clínica mediante entrenamientos dirigidos a investigadores, coordinadores y equipos de estudio involucrados en la gestión y ejecución de ensayos clínicos.

Es una plataforma internacional de formación certificada en Buenas Prácticas Clínicas, dirigida a investigadores y equipos de investigación clínica de Cayetano Heredia.
Para llevar el curso contactar a: duari.ocri@oficinas-upch.pe

Entrenamiento online especializado en Buenas Prácticas Clínicas: gratuito.
Equipo y contacto
Contacto: duari.ensayosclinicos@oficinas-upch.pe
Oficina de Ensayos Clínicos
Av. Honorio Delgado 430, Urb. Ingeniería, Lima – Perú
duari.ensayosclinicos@oficinas-upch.pe
(511) 319-0000 | Anexo 201354